
Votre question concerne quel type d'offre ?
Votre question concerne quel couloir Ségur ?
Votre question concerne quel dispositif Ségur ?
Votre question concerne quel produit ou service produit?
Votre question concerne quelle thématique ?
Le système MSSanté est un système de messagerie qui permet d’échanger par mail de façon sécurisée des données de santé à caractère personnel entre professionnels habilités, dans le cadre de la prise en charge d'un patient. A ce jour, les données de facturation ne rentrent pas dans ce périmètre.
Cette réponse vous a-t-elle été utile ?
Seul un exploitant peut candidater sur la plateforme Convergence. Un exploitant peut être le fabricant (si possède une entité en France) ou un distributeur (dans le cas ou le fabricant ne peut pas être l'exploitant, c'est à dire qu'il ne possède pas entité juridique en France).
Si le distributeur ne peut pas obtenir de certificat, alors c'est le fabricant qui sera remboursé et le distributeur devra passer un accord de distribution avec le fabricant.
Cette réponse vous a-t-elle été utile ?
Non, cela n'est pas nécessaire : un seul formulaire 413 est suffisant pour commander les certificats DMP et INSi. Il vous faut cocher la case "Certificat ORG (personne morale)", puis indiquer dans la case "Précisions sur l’usage des certificats et sur votre projet" les informations suivantes:
DMP: authentification et signature sur le DMP ;
INSI: authentification sur les TLS INSi.
Cette réponse vous a-t-elle été utile ?
Le système désigne le LGO donc la visualisation doit se faire au travers du LGO. En revanche, comme il s'agit d'une préconisation, le développement de cette fonctionnalité n'est pas obligatoire pour le référencement vague 1. Elle le deviendra pour la vague 2.
Cette réponse vous a-t-elle été utile ?
Le SGL doit faire 1 et 2, pour faire face à toutes les situations :
- capable de fournir ‘directement’ au client une alimentation DMP
- soit le SGL alimente directement le DMP, il faut que le SGL apporte sa propre homologation CNDA ;
- soit le SGL a une PFI (‘module’) sous-traitant qui s’en charge (PFI invisible pour le client), il faut alors qu’il apporte l’homologation CNDA du sous-traitant (et nous donne quelques éléments sur son interconnexion en sortie avec son ‘module’) lors du référencement de l’ensemble [SGL + module] (1 seul référencement) ;
et
- capable de laisser l’hôpital gérer les envois au DMP avec la PFI de l'hôpital (non choisie par le SGL, mais préalablement choisie par l’hôpital). Il n'appartient pas au SGL de s'assurer que la PFI est référencée Ségur. Le SGL n’a aucune homologation CNDA à apporter dans ce cas. Le SGL doit en revanche prouver qu’il sait envoyer les CR par des messages ORU (qui seront routés par la DSI vers la PFI hospitalière)
Cette réponse vous a-t-elle été utile ?
Les exigences sur la eprescription couvre l'ensemble des prescriptions détaillées en annexe 3 du DSR.
Cette réponse vous a-t-elle été utile ?
Non, chaque preuve doit être déposée séparément dans le formulaire en suivant scrupuleusement les formats imposés.
Cette réponse vous a-t-elle été utile ?
Les choix d'ergonomie sont laissés à la discrétion des industriels.
La trace des résultats modifiés/ supprimés sont à rendre accessibles à l’utilisateur en cas de modification et de suppression.
Cette réponse vous a-t-elle été utile ?
Oui, il est prévu d'utiliser un certificat serveur pour transmettre les messages.
Cette réponse vous a-t-elle été utile ?
Les exigences suivantes sont dans le DSR SGL vague 1 :
- le système DOIT savoir produire automatiquement le CR Bio en CDA R2 N3, conformément au volet Compte Rendu d'Examen de Biologie du CI-SIS [CISIS3] ;
- le système PEUT produire automatiquement le CR Bio avec une version unique ou deux versions, patient et professionnel (dans le cadre d'un paramétrage général), en CDA R2 N3, conformément au volet Compte Rendu d'Examen de Biologie du CI-SIS [CISIS3] ;
- le système DOIT savoir produire le CR Bio sous format CDA R2 N1 avec un PDF encapsulé en base 64, conformément au volet Structuration Minimale du CI-SIS [CISIS1] ;
- le système DOIT permettre par défaut l'envoi systématique et automatique du compte rendu d'examen de biologie dans la version conforme au volet Compte Rendu d'Examen de Biologie du CI-SIS [CISIS3] et dans la version conforme au Volet Structuration Minimale du CI-SIS [CISIS1]) au DMP dès la validation biologique, y compris pour les CR Bio produits au sein de séjours hospitaliers.
Il faut comprendre qu’il faut, dans le cas où il y a deux versions, envoyer les deux au DMP, donc potentiellement 4 documents N1/N3 patient/pro. Conformément au RGPD, sauf pour les cas de consultation d’annonce, il ne faut pas mettre de masquage patient sur la version 'professionnelle' du compte-rendu.
Cette réponse vous a-t-elle été utile ?
Sauf cas exceptionnel, un DMN ne doit candidater que sur un seul parcours (ligne générique ou nom de marque). Par contre, dans le cas ou un DMN traite de plusieurs pathologies (dont une incluse dans les lignes génériques), l'industriel peut candidater sur les deux parcours. Les différents dossiers correspondants sont indépendants et peuvent être déposés simultanément. Dans le cas où des preuves seraient communes, merci de le signaler à l'ANS afin de pouvoir optimiser le traitement des dossiers.
Cette réponse vous a-t-elle été utile ?
L'ANS a 60 jours calendaires pour certifier conforme une solution à partir du moment où l'ensemble des preuves aura été déposé, hors allers/retours éventuels en cas de preuves KO ou incomplètes. Il est donc difficile de donner un délai, qui dépend également de la réactivité de l'Entreprise du Numérique en Santé.
Cette réponse vous a-t-elle été utile ?
L'attribution d'un certificat de conformité se fait après la validation du formulaire de recevabilité, et l'analyse par l'ANS des preuves déposées dans Convergence. Une fois le certificat de conformité attribué, l'ANS se réserve le droit d'effectuer (ou de faire effectuer par un prestataire) des audits de conformité aux ENS certifiés.
Ces audits se déroulent en général dans un environnement de test.
Cette réponse vous a-t-elle été utile ?
Dans le cadre d'une prestation de télésurveillance faisant intervenir un prestataire, c'est bien au fournisseur de la machine de ventilation de déposer un dossier pour la certification de conformité pour une inscription en ligne générique.
Le prestataire n'a généralement pas le rôle d'un opérateur, mais il pourrait potentiellement être amené à facturer à la place de l’exploitant s’il assume toute les responsabilités qui lui incombe dans le cadre de la délégation de tâche.
Il est malgré tout préférable qu'il y ait un code par solution numérique, et donc que ce soit le fabricant qui fasse la démarche simplifiée pour un code individuel.
En résumé, une activité de télésurveillance c'est :
- un forfait opérateur (donc à obtenir par l'opérateur de télésurveillance) ;
- un forfait technique (à obtenir par le fabriquant).
Pour tout complément d'information, nous vous invitons à poser vos questions à l'adresse suivante : dss-sd1c@sante.gouv.fr.
Cette réponse vous a-t-elle été utile ?
Si la modification apportée ne remet pas en cause la conformité du DMN aux Exigences (par ex. patch correctif, etc.), la certification bénéficie au Logiciel modifié, sans qu’il soit nécessaire de déposer une nouvelle demande de certification relative à celui-ci ou de procéder à une quelconque notification auprès de l’Agence du numérique en santé. Si la modification apportée affecte la conformité du DMN aux Exigences, l’Agence du Numérique en Santé doit en être notifiée par l’Editeur dans un délai de 15 jours. Cette information est accompagnée de tout élément permettant de documenter la nature de la modification et les Exigences de conformité impactées. En réponse, l’ANS peut demander à l’Editeur de déposer une nouvelle demande de certification dans un délai d’un mois.
Cette réponse vous a-t-elle été utile ?
Les sanctions seront graduées en fonctions des manquements constatés, de plus la LFSS 2023 va renforcer le pouvoir de sanction de l’agence en y ajoutant la possibilité de sanctions financières.
Cette réponse vous a-t-elle été utile ?
Afin d’optimiser le temps d’obtention du certificat de conformité au référentiel des DMN de l’ANS, l’entreprise de numérique en santé peut anticiper un certain nombre de démarches, qui seront nécessaires lors du dépôt des preuves. Il s’agit des démarches en vue de l’homologation CNDA au téléservice INSi, dans le cas où le DMN est référentiel d’identité. Il faut, en amont de la certification de conformité :
- Commander des cartes CPs/CPE de test, le cas échéant
Téléchargez le formulaire - Commander un certificat logiciel, le cas échéant
Téléchargez le formulaire - Demander l’homologation auprès du CNDA
Consultez le site du CNDA
En aval de la certification, il faudra ensuite :
- Déposer un dossier auprès de la CNEDIMS le cas échéant (pour les demande en nom de marque)
Rendez-vous sur le site de la HAS - Faire la demande d’obtention du code de remboursement auprès du ministère sur le site
Consultez le site des démarches simplifiées
Cette réponse vous a-t-elle été utile ?
Afin d'optimiser les temps de traitement et de sécuriser l'ensemble de la conformité de la candidature, il est recommandé de n'en déposer qu'une seule. Dans ce cas, il vous faut déposer une preuve par application le cas échéant, si les interfaces et les fonctionnalités sont différentes.
Cette réponse vous a-t-elle été utile ?
Oui, il est possible de répondre aux exigences du référentiel grâce à une solution tierce. En effet, par exemple, l'homologation CNDA pour l'appel au téléservice INSi peut être obtenue par une application tierce complémentaire à votre dispositif médical numérique.
Cette réponse vous a-t-elle été utile ?
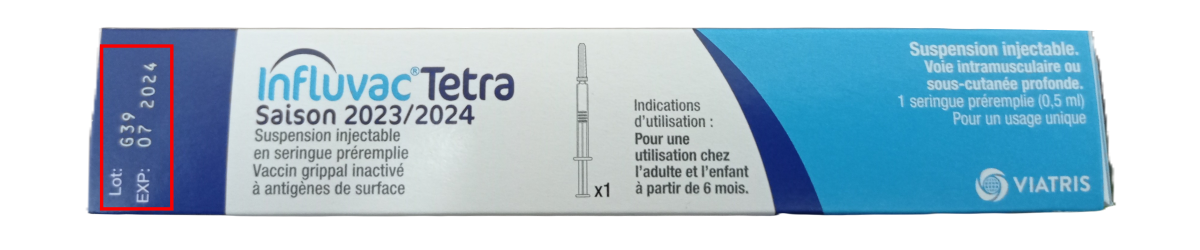
Vous trouverez ci-dessous, une image d’une boite de vaccin qui vous permettra de répondre à l’exigence ERGO 4 et sur laquelle vous trouverez le numéro de lot, la date d’expiration, le Datamatrix ainsi que le nom du vaccin qui doit ressortir dans votre logiciel.


Cette réponse vous a-t-elle été utile ?


